

Orientador(a): Márcio Antonio Brunetto
Instituição: FMVZ USP
Trabalho classificado na 9ª Edição (2023) do Prêmio de Pesquisa PremieRpet®.
Índice
Resumo
A pancreatite é definida como a inflamação do pâncreas exócrino e é a enfermidade pancreática mais frequente em cães. A patogenia envolve a ativação prematura, intra-acinar do tripsinogênio em tripsina que ativa cascata enzimática envolvida no processo inicial de autodigestão do tecido pancreático e peripancreático, ocasionando injúria tecidual, aumento da permeabilidade vascular e pode culminar em isquemia e necrose. O tratamento consiste em fluidoterapia e terapêutica sintomática, visto que a causa pode não ser elucidada. O suporte nutricional poderá ser instituído através da nutrição enteral ou parenteral. Antigamente, a suspensão do fornecimento de água e alimentação parecia ser benéfica em pacientes com pancreatite, uma vez que coibiria a estimulação pancreática. No entanto, essa prática é questionável, pois estudos demonstraram que existem evidências de que a alimentação precoce é de suma importância na recuperação desses animais, em razão da presença de alimento no intestino estabilizar a função de barreira gastrointestinal, evitar a translocação bacteriana, auxiliar na nutrição dos enterócitos, manter a função imunitária, aumentar a motilidade intestinal, previnir o catabolismo e diminuir o tempo de hospitalização. A presente revisão objetivou avaliar o efeito da instituição precoce de suporte nutricional em cães diagnosticados com pancreatite e concluiu que a nutrição precoce, sobretudo enteral, é segura e bem tolerada. Além disso, sua instituição auxilia de forma positiva no retorno da ingestão alimentar voluntária e pode favorecer a manutenção da função de barreira intestinal.
Introdução
A pancreatite é definida como a inflamação do pâncreas exócrino e é a enfermidade pancreática mais diagnosticada em cães (BERMAN; LOBETTI; LINDQUIST, 2020). A patogenia envolve a ativação prematura, intra-acinar do tripsinogênio em tripsina que ativa a cascata enzimática envolvida no processo inicial de autodigestão do tecido pancreático e peripancreático. Esse processo ocasiona injúria tecidual, aumento da permeabilidade vascular e pode culminar em isquemia e necrose (SILVA; PONCE, 2015).
Fatores como hiperlipidemia, hipercalcemia, reações adversas a medicamentos, toxinas, perfil da dieta, traumatismos, lesões por reperfusão, endocrinopatias e condições infecciosas podem predispor à pancreatite, contudo, a maioria dos casos em cães é considerada idiopática (SILVA; PONCE, 2015).
O diagnóstico é desafiador, uma vez que as características clínicas são variáveis e inespecíficas e não existe uma metodologia padrão ouro universalmente aceita (LIDBURY; SUCHODOLSKI, 2016). Alguns animais podem apresentar êmese, dor abdominal e “posição de prece”, além de anorexia, prostração e desidratação (VAN DEN BOSSCHE; PAEPE; DAMINET, 2010; KALLI et al., 2017).
Os achados laboratoriais geralmente consistem em anemia, leucocitose por neutrofilia, trombocitopenia, azotemia pré-renal, aumento da atividade sérica de enzimas hepáticas (alanina aminotransferase e fosfatase alcalina), hiperbilirrubinemia e alterações eletrolíticas (SILVA e PONCE, 2015). A lipase pancreática canina específica (cPL) é um método sensível e apresenta boa correlação nos casos de pancreatite (SILVA; PONCE, 2015). Contudo, as concentrações podem estar aumentadas em outras enfermidades, incluindo gastroenterite por parvovírus (KALLI et al., 2017), erliquiose monocítica canina (MILONAKIS et al., 2014), corpos estranhos (SPINELLA et al., 2018), dilatação vólvulo-gástrica (COCHRAN et al.,2016), doença renal crônica (CRIDGE et al., 2020), doença mixomatosa da válvula mitral (PARK et al., 2019), cetoacidose diabética (BOLTON et al., 2016) e síndrome de cushing (KIM et al., 2019).
Ultrassonograficamente, o pâncreas poderá se apresentar hipoecóico e o mesentério peripancreático hiperecoico. Alterações em órgãos adjacentes também poderão ser visibilizadas, incluindo dilatação ou obstrução de vias biliares e duodenite (SILVA; PONCE 2015; PALERMO et al., 2020). Todavia, a ausência desses achados não descarta a enfermidade (MANSFIELD, 2012). O padrão ouro é o exame histopatológico que, por ser uma técnica invasiva e perigosa, acaba não sendo empregado (HULSEBOSCH et al., 2016).
O tratamento consiste em fluidoterapia, que objetiva corrigir distúrbios hidroeletrolíticos e acido-básicos e reestabelecer a hemodinâmica do paciente, associado a analgésicos, antieméticos, protetores gástricos e, em casos em que a infecção for evidente (leucocitose por neutrofilia, desvio a esquerda, neutrófilos tóxicos, hemocultura positiva), a antibioticoterapia é recomendada. A terapêutica geralmente é sintomática, visto que a causa pode não ser elucidada (SILVA; PONCE, 2015).
O suporte nutricional poderá ser instituído através da nutrição enteral ou parenteral. A nutrição enteral baseia-se na administração de nutrientes por meio do trato gastrointestinal por via oral via alimentação forçada ou através de sondas de alimentação (VEADO, 2017). Considera-se que a nutrição enteral precoce é aquela que acontece em até 48hs após a internação, ainda que seja recomendável seu início de maneira mais breve possível, nas primeiras 24 horas. A nutrição parenteral refere-se à administração de nutrientes por via intravenosa, pela via periférica (parcial) ou central (parcial ou total). A nutrição parenteral total fornece todos os constituintes energéticos em sua formulação e, por exigir acesso venoso central, necessita de manutenção rigorosa e profissionais capacitados para sua realização. Enquanto que a periférica ou parcial é menos onerosa e possui menos complicações, porém, os nutrientes são fornecidos com ausência de caracterização prévia da formulação, dependendo apenas do limite da osmolaridade dos acessos periféricos (ROMBEAU, 2004).
Antigamente, a suspensão do fornecimento de água e alimentação parecia ser benéfica em pacientes com pancreatite, pois coibiria a estimulação pancreática. Recomendava-se, portanto, jejum absoluto de 48 a 72 horas ou mais (MANSFIELD, 2012). No entanto, essa prática é questionável, pois estudos demonstraram que existem evidências de que a alimentação precoce é de suma importância na recuperação desses animais (MASNFIELD, 2012; JENSEN; CHAN, 2014).
A presença de alimento no intestino estabiliza a função de barreira gastrointestinal, evita a translocação bacteriana, auxilia a saúde dos enterócitos, mantém a função imunitária, aumenta a motilidade intestinal, previne o catabolismo e diminui o tempo de hospitalização (MASFIELD, 2012; JENSEN e CHAN, 2014).
A presente revisão objetivou avaliar o efeito da instituição precoce de suporte nutricional em cães diagnosticados com pancreatite.
Desenvolvimento
Para esta revisão, os trabalhos foram procurados por meio das palavras- chave “pancreatitis”, “dogs” e “nutrition”, associadas ao operador booleano AND, de maneira que trabalhos que apresentassem todas as palavras supramencionadas fossem incluídos, restringindo a amplitude da pesquisa. Esta estratégia de busca abrangeu as bases de dados eletrônicas Embase, PubMed, Scopus e BVS-Vet.
A escolha do tema foi baseada no questionamento quanto aos efeitos do suporte nutricional precoce em casos de pancreatite em cães, associado à grande casuística dessa enfermidade nos atendimentos clínicos de pequenos animais (WATSON et al., 2015)
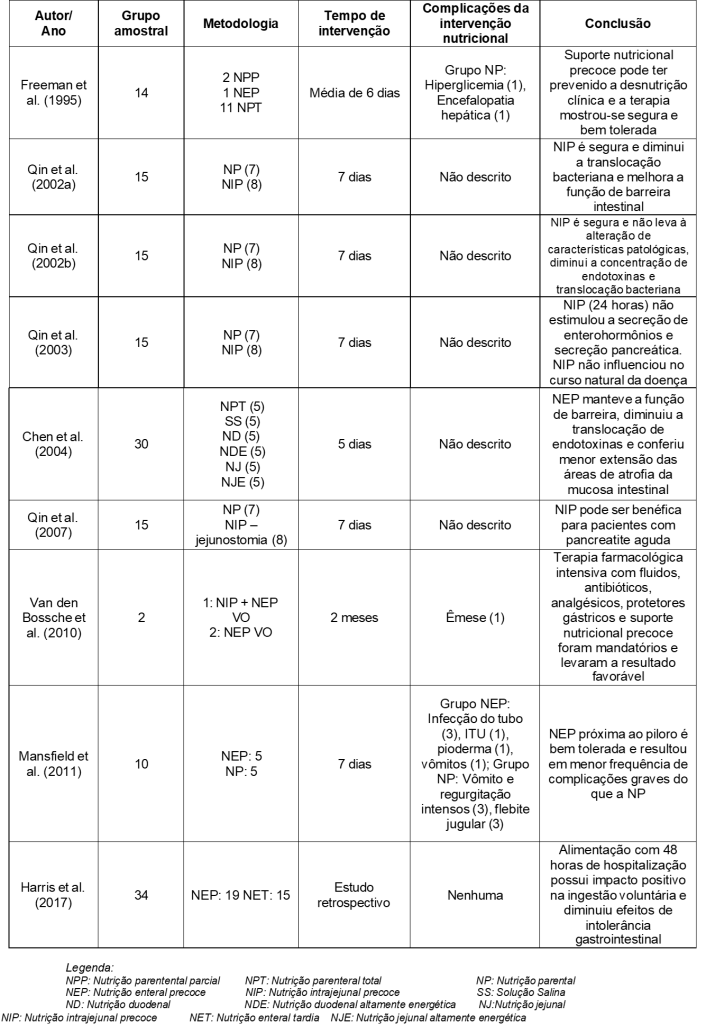
Os resultados descritos na Tabela 1 demonstram que o grupo amostral, a metodologia utilizada e o tempo de tratamento foram extremamente variáveis. Todavia, todos concluíram que o uso da nutrição precoce é benéfica em cães diagnosticados com pancreatite.
A presença de alimento no estômago estimula a função exócrina em pacientes com pancreatite aguda, fato que justifica alguns autores optarem pela nutrição intrajejunal (QIN et al., 2002a, QIN et al., 2002b, QIN et al., 2003, QIN et al., 2007). Porém, a instituição de nutrição enteral via oral, próxima ao piloro e duodenal mostrou-se eficaz em diversos aspectos, além de não haver exacerbação de algia ou quadros eméticos no grupo alimentado por via enteral, em comparação ao grupo em que a via parenteral foi utilizada (QIN et al., 2002a, MANSFIELD et al., 2011).
A nutrição enteral é a rota mais natural para administração de nutrientes e sabidamente melhora a integridade e função de mucosa intestinal (QIN et al., 2002a; QIN et al., 2003; HARRIS et al., 2017). Não obstante, a sintomatologia clínica associada a não integridade intestinal (melena, hematoquezia, regurgitação) presenciados após a não ingestão de alimentos por mais de 3 dias são fatores prognósticos negativos em casos de pancreatite em cães e demonstra a importância do suporte nutricional precoce nesses pacientes (VAN DEN BOSSCHE; PAEPE; DAMINET, 2010).
Apesar da nutrição enteral ser bem tolerada e benéfica, o tipo de alimento a ser oferecido ainda é uma incógnita. Os cães com pancreatite geralmente são alimentados com uma dieta com restrição de gordura. Contudo, James et al. (2009) concluíram que, em cães saudáveis, não houve diferença significativa na adaptação pancreática mensurável em cães alimentados com teor variável de gordura, questionando a essencialidade do uso desse tipo de dieta. Indubitavelmente, em pacientes diagnosticados com hiperlipidemia, é recomendável optar por alimentos com baixo teor de gordura (MANSFIELD et al., 2012). A associação entre hiperlipidemia e pancreatite permanece incerta em cães, mas presume-se que seja bidirecional (XENOULIS; STEINER 2015). A hiperlipidemia tem sido considerada uma etiologia da pancreatite em cães e humanos. Por outro lado, o aumento dos lípideos também foi hipotetizado como resultado da inflamação pancreática, mas este fato ainda é questionável, pois pode haver etiologia multifatorial, como resultado da própria pancreatite, comorbidades, estado pós-prandial ou uma combinação desses fatores (WHITNEY et al., 1987, COOK et al., 1993; XENOULIS et al., 2020).Em um estudo conduzido por Xenoulis (2020), 70% dos cães apresentava concentrações séricas de triglicerídes e colesterol normais, sendo improvável que aumentos acentuados nas concentrações séricas de lípideos em cães com pancreatite sejam o resultado da inflamação e justifiquem investigação diagnóstica adicional. Ainda no mesmo estudo, foram identificadas discrepâncias entre os perfis de lipoproteínas entre cães com pancreatite e cães controles saudáveis, com concentrações de LDL mais altas e frações TRL e HDL mais baixas do que no grupo controle. Entretanto, mais estudos são necessários para determinar o papel desses metabólitos na pancreatite (XENOULIS et al., 2020).
Em suma, em humanos, ensaios clínicos comprovaram que houve diminuição de complicações inflamatórias por meio do uso de nutrição enteral precoce em comparação a nutrição parenteral (MARIK; ZALOGA, 2004; MANSFIELD et al., 2011). Na medicina veterinária, melhor resposta clínica foi atribuída ao suporte enteral precoce, pois reduziu o catabolismo proteico, preveniu a desnutrição proteico-energética, melhorou a integridade epitelial e diminuiu a inflamação intestinal (LIU; BROWN; SILVERSTEIN, 2012).
Considerações finais
A nutrição precoce, sobretudo enteral, é segura e bem tolerada. Sua instituição auxilia de forma positiva no retorno da ingestão alimentar voluntária e pode favorecer a manutenção da função de barreira intestinal. Tais achados sugerem que seus efeitos são benéficos em cães diagnosticados com pancreatite.
Referências bibliográficas
BERMAN, C.F.; LOBETTI, R.G.; LINDQUIST, E. Comparison of clinical findings in 293 dogs with suspect acute pancreatitis: Different clinical presentation with left lobe, right lobe or diffuse involvement of the pancreas. J S Afr Vet Assoc. 2020, v.91, e1-e10, 2020.
BOLTON, T.A.; COOK, A.; STEINER, J.M.; FOSGATE, G.T. Pancreatic lipase
immunoreactivity in serum of dogs with diabetic ketoacidosis. J Vet Intern Med, v. 30, n.4, p.958-963, 2016.
CRIDGE, H.; TWEDT, D.C.; MAROLF, A.J.; SHARKEY, L.C.; STEINER,
J.M. Advances in the diagnosis of acute pancreatitis in dogs. J Vet Intern Med., v.35,
- 6, p.2572- 2587, 2020.
COCHRAN, L.; HILL, S.; SUCHODOLSKI, J.S, et al. Imunorreatividade da lipase pancreática sérica em cães com corpos estranhos gástricos (Resumo: fórum ACVIM 2016) . J Vet Intern Med, v.30, n. 1453, 2016.
CHEN, J.; WANG, X.P.; LIU, P.; WU, K.; XU, M.; YU, X.F.; WANG, G.S. Effects of
continuous early enteral nutrition on the gut barrier function in dogs with acute necrotizing pancreatitis. Zhonghua Yi Xue Za Zhi, v.84, n.20, p.1726-31, 2004.
FREEMAN, L M.; LABATO, M A.; RUSH, J E.; MURTAUGH, R J. Nutritional Support
In Pancreatitis: A Retrospective Study. Journal of Veterinary Emergency and Critical Care. v. 5, n.1, p.32-41, 1995.
HARRIS, J.P.; PARNELL, N.K.; GRIFFITH, E.H.; SAKER, K.E. Retrospective
evaluation of the impact of early enteral nutrition on clinical outcomes in dogs with pancreatitis: 34 cases (2010-2013). J Vet Emerg Crit Care, v. 27, n.4,p.425-433, 2017.
HULSEBOSCH, S.E.; PALM, C.A.; SEGEV, G.; COWGILL, L.D.; KASS, P.H.;
MARKS, S.L. Evaluation of Canine Pancreas-Specific Lipase Activity, Lipase Activity, and Trypsin-Like Immunoreactivity in an Experimental Model of Acute Kidney Injury in Dogs. J Vet Intern Med, v. 30, n.1, p. 192-199, 2016.
JAMES, F.E.; MANSFIELD, C.S.. STEINER, J.M.; WILLIAMS, D.A.; ROBERTSON,
I.D. Pancreatic response in healthy dogs fed diets of various fat compositions. Am J Vet Res v.70, p.614 – 618, 2009.
JENSEN, K. B.; CHAN, D. L. Nutritional management of acute pancreatitis in dogs and cats. J Vet Emerg Crit Care, p. 1–11, 2014.
KALLI, I.V.; ADAMAMA-MORAITOU, K.K.; PATSIKA, M.N. et al. Prevalence of
increased canine pancreas-specific lipase concentrations in young dogs with parvovirus enteritis. Veterinary Clinical Pathology, v.46, p.111–119, 2017.
KIM, H.; KANG, J.H.; HEO, T.Y et al. Evaluation of hypertriglyceridemia as a mediator between endocrine diseases and pancreatitis in dogs. J Am Anim Hosp Assoc. v.55, n.2, p.92-100, 2019.
LIDBURY, J.A; SUCHODOLSKI, J.S. New advances in the diagnosis of canine and feline liver and pancreatic disease. Vet J, v. 215, p.87-95, 2016.
MANSFIELD, C. S. Acute pancreatitis in Dogs: Advances in Understanding, Diagnostics, and Treatment. Topics in Companion Animal Medicine, v. 27,p. 122- 132, 2012.
MANSFIELD, C.S.; JAMES, F.E.; STEINER, J.M. et al. A pilot study to assess tolerability of early enteral nutrition via esophagostomy tube feeding in dogs with severe acute pancreatitis. J Vet Intern Med, v.25, p.419–425, 2011.
MARIK, P.E.; ZALOGA, G.P. Meta-analysis of parenteral nutrition versus enteral nutrition in patients with acute pancreatitis. Br Med J, v.328,p.1407–1412, 2004.
MYLONAKIS M.E.; XENOULIS, P.G.; THEODORU, K. et al. Imunorreatividade da lipase pancreática canina sérica na erliquiose monocítica canina ( Ehrlichia canis) induzida experimentalmente e de ocorrência natural . Vet Microbiol, v. 169, p.198-202, 2014.
NELSON, R. W.; COUTO, C. G. O Pâncreas exócrino. Medicina interna de pequenos animais. 5.ed. Rio de Janeiro: ELSEVIER, 2015. p. 1772 – 1825.
PARK, J.S.; PARK, J.H.; SEO, K.W.; SONG, K.H. Correlation between NT-proBNP and lipase levels according to the severity of chronic mitral valve disease in dogs. J Vet Sci, v.20,n.4, 2019.
QIN, H. L.; SU, Z. D.; HU, L. G.; DING, Z. X.; LIN, Q. T Effect of parenteral and early intrajejunal nutrition on pancreatic digestive enzyme synthesis, storage and discharge in dog models of acute pancreatitis. World journal of gastroenterology,v.13, n.(7),p. 1123–1128, 2007.
QIN, H. L.; SU, Z. D.; HU, L. G.; DING, Z. X.; LIN, Q. T Parenteral versus early intrajejunal nutrition: effect on pancreatitic natural course, entero-hormones release and its efficacy on dogs with acute pancreatitis. World journal of gastroenterology, v.9, n.10,p. 2270–2273, 2003.
QIN, H.L.; SU, Z.D.; HU, L.G.; DING, Z.X.; LIN, Q Early intrajejunal nutrition: Bacterial translocation and gut barrier function of severe acute pancreatitis in dogs. Hepatobiliary Pancreat Dis Int. n.1, v.1, p.150-4, 2002a.
QIN, H.L.; SU, Z.D.; HU, L.G.; DING, Z.X.; LIN, Q.T.Effect of early intrajejunal nutrition on pancreatic pathological features and gut barrier function in dogs with acute pancreatitis. Clinical Nutrition, v.21, n.6, p. 469-473, 2002b.
ROMBEAU, J.L.; ROLANDELLI, R.H. Nutrição clínica: Nutrição parenteral. 3a ed. São Paulo: Roca, 2004.
SILVA, R.D.; PONCE, F.G. Pancreatite. In: JERICÓ, M.M; NETO, J.P.A.; KOGIKA,
M.M. Tratado de medicina interna de cães e gatos. Rio de Janeiro: Roca, 2015. p. 1047-1052.
VAN DEN BOSSCHE, I; PAEPE, D.; DAMINET, S. Acute pancreatitis in dogs and cats: pathogenesis, clinical signs and clinicopathologic findings. Vlaams Diergeneeskundig Tijdschrift, v.79, p.13-22, 2010.
XENOULIS, P.G.; CAMMARATA, P.J.; WALZEM, R.L; SUCHODOLSKI, J.S.;
STEINER, J.M. Serum triglyceride and cholesterol concentrations and lipoprotein profiles in dogs with naturally occurring pancreatitis and healthy control dogs. J Vet Intern Med, v.34, n.2, p.644-652, 2020.






